AR作为前列腺癌治疗的重要靶点之一,其持续的下游信号传导对前列腺癌(PC)以及去势抵抗性前列腺癌(CRPC)的发生和发展起着重要作用。通过药物阻断雄激素与AR的结合是治疗PC与CRPC的有效手段,然而,以AR拮抗剂恩杂鲁胺为代表的一线疗法通常不仅缺乏肿瘤靶向性,而且会因AR突变而引起药物毒性及耐药作用。因此,利用新的药物设计策略,特异性阻断肿瘤中的AR的信号通路,将有望在治疗前列腺癌中发挥重要作用。近日,秦冲教授团队在靶向雄激素受体(AR)的小分子降解剂研究领域连续取得新进展,在国际药物化学领域顶级期刊《Journal of Medicinal Chemistry》上发表两篇研究性论文。
热休克蛋白90(Heat shock protein 90,Hsp90)是真核生物中一种非常重要的蛋白质。研究发现,肿瘤细胞中的Hsp90表达水平会异常升高,并发挥重要作用,主要表现为两个方面:(1)Hsp90会分泌至肿瘤细胞膜表面(extracellular Hsp90, eHsp90),促进肿瘤的迁移、侵袭和转移,并具备介导内吞的作用;(2)Hsp90通过分子伴侣功能来调控肿瘤细胞内的蛋白水平。AR作为Hsp90的客户蛋白,受后者的功能调控,当Hsp90的功能受到抑制时,AR的正常折叠过程将被终止,并被E3泛素连接酶进行泛素化标记,进而被蛋白酶体降解。基于上述背景,研究人员提出了将Hsp90抑制剂和AR拮抗剂通过共价连接,构建偶联物分子的设想。
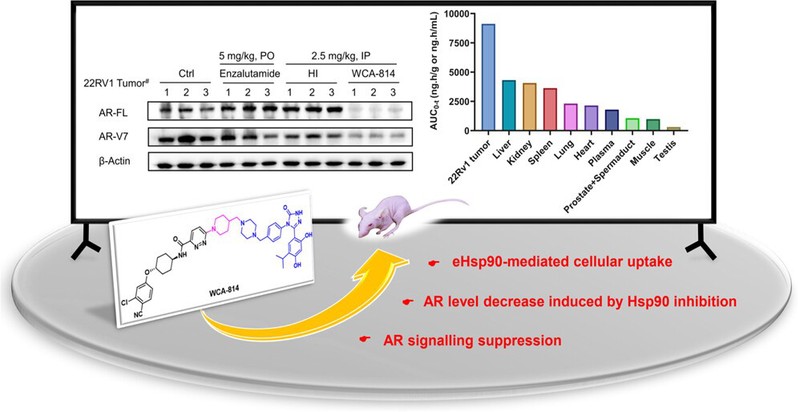
图1. AR拮抗剂-Hsp90抑制剂偶联分子WCA-814的结构与活性研究
研究人员通过初步细胞活性筛选得到AR拮抗剂-Hsp90抑制剂偶联分子WCA-814,其在低纳摩尔的给药浓度下能有效抑制去势抵抗性前列腺癌细胞系LNCaP和22Rv1的增殖,并能够以剂量依赖性和时间依赖性的方式显著诱导AR-FL和剪切突变体AR-V7的降解。
候选化合物WCA-814(2.5 mg/kg,IP)在恩杂鲁胺耐药型22Rv1动物CDX模型中表现出优于AR拮抗剂恩杂鲁胺(5 mg/kg,PO)和Hsp90抑制剂HI(2.5 mg/kg,IP)的肿瘤生长抑制活性,并能显著下调肿瘤组织中的AR-FL和AR-V7表达水平。22Rv1模型中WCA-814的组织分布结果显示,其在肿瘤中的药物暴露量是血液和其他正常组织器官的2-5倍以上,表明化合物具有较高的肿瘤靶向性。当给药窗口提升10倍,持续14天后,WCA-814并未对小鼠的组织器官产生明显影响,进一步证明了化合物的安全性。
此外,蛋白水解靶向嵌合体(PROTAC)是一种有前景的双功能分子,它通过劫持细胞中泛素-蛋白酶体系统(UPS)来诱导靶蛋白的泛素化,随后通过蛋白酶体降解。虽然许多靶向AR-LBD(配体结合结构域)PROTACs已经成功地实现了AR的降解,但这些PROTACs针对AR-V7的降解效力仍然较弱。由于AR-FL和AR-V7都保留了N末端转录结构域(NTD),因此靶向AR-NTD的PROTACs能够同时结合并降解AR-FL和AR-V7,消除其功能,在治疗PC和CRPC中具备临床价值。综上,研究人员开展了首个靶向AR-NTD的PROTACs设计、合成和生物学评价的研究。
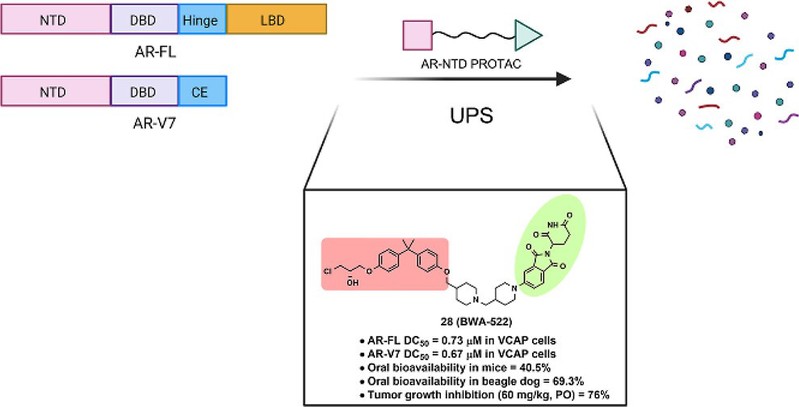
图2. AR-NTD PROTAC分子BWA-522的结构与活性研究
研究人员选择AR-NTD拮抗剂EPI-002作为靶蛋白配体,E3连接酶VHL与CRBN的配体作为招募E3配体,通过不同Linker将两部分连接。通过降解活性初筛,BWA-522被作为候选分子进行接下来的研究。在随后PK测试中,研究人员发现化合物BWA-522具有良好的口服血浆暴露,AUC值为5947 h·ng/ml,且口服生物利用度为40.5%。鉴于BWA-522在小鼠中优秀的口服利用度,我们进一步评估了其在比格犬中的PK。当口服剂量为5 mg/kg时,BWA-522的t1/2为31.2 h,口服生物利用度为69.3%。这些结果共同表明BWA-522是一种具备口服活性的分子。
研究人员评估了口服BWA-522对LNCaP异种移植肿瘤模型小鼠的抗肿瘤能力。结果显示,与对照组相比,口服20和60 mg/kg BWA-522对肿瘤生长的抑制率分别为26%和76%,表现出优于AR-NTD拮抗剂EPI-002(180 mg/kg,PO)的肿瘤抑制活性。此外,研究人员还进行了BWA-522毒理研究,以评估其在ICR小鼠中的潜在副作用。BWA-522以20和60 mg/kg的剂量每日口服给药,连续14天。在治疗结束时,两剂量组均未观察到明显的动物体重减轻或器官损伤,表明BWA-522在体内具有良好的体内耐受性。
综上,秦冲教授课题组发现的两类小分子AR降解剂具备进一步开发为候选药物的潜力,为研发治疗前列腺癌的药物提供了新的思路。
金沙3777官方网站为本论文的第一完成单位,秦冲教授为通讯作者,学院博士后张思琪,硕士研究生孟晓蕾和工程师张赛为第一篇论文共同一作;博士研究生张博闻,硕士研究生刘畅、杨振乾和工程师张赛为第二篇论文共同一作。相关工作得到国家重点研发计划、国家自然科学基金及山东省自然科学基金优秀青年基金等项目的资助。
文章链接:
① https://pubs.acs.org/doi/full/10.1021/acs.jmedchem.2c01970
② https://pubs.acs.org/doi/full/10.1021/acs.jmedchem.3c00585
【关闭】





